.
Às vezes, o número de telas que você vê por dia supera o número de rostos humanos. Não é irônico que as ferramentas que você usa para se conectar também possam fazer você se sentir mais isolado? Em vez de ser parte do problema, a tecnologia pode ser parte da solução.
Entre no ChatGPT, o chatbot que não se trata apenas de responder perguntas triviais aleatórias ou definir lembretes. É capaz de ouvir, dar conselhos e, com isso, fazer você se sentir menos solitário. Antes de revirar os olhos, explore como você pode usar o ChatGPT de maneira mais eficaz para combater a solidão.
Engenharia de Prompt para Conversas ChatGPT
Você já deve ter usado IA para combater a solidão, e os companheiros de bate-papo com IA online podem ser ferramentas úteis quando as interações reais são limitadas. Você também pode já ter usado o ChatGPT como treinador de saúde mental ou para desenvolver inteligência emocional. Como uma grande ferramenta de modelo de linguagem, é capaz de imitar muitos tipos de conversas.
O truque para usar o ChatGPT de maneira eficaz para combater a solidão está no prompt. Pense na engenharia imediata como a diferença entre perguntar a alguém: “Como foi seu dia?” versus “Conte-me a coisa mais interessante que aconteceu com você hoje”. Este último certamente provocará uma resposta mais envolvente. Da mesma forma, com o ChatGPT, a mágica está nas instruções.
Vamos mergulhar na variedade de personalidades que você pode criar. Quem sabe, você pode até criar um prompt de uma forma que torne o ChatGPT tão envolvente que você pode esquecer que está falando com a IA.
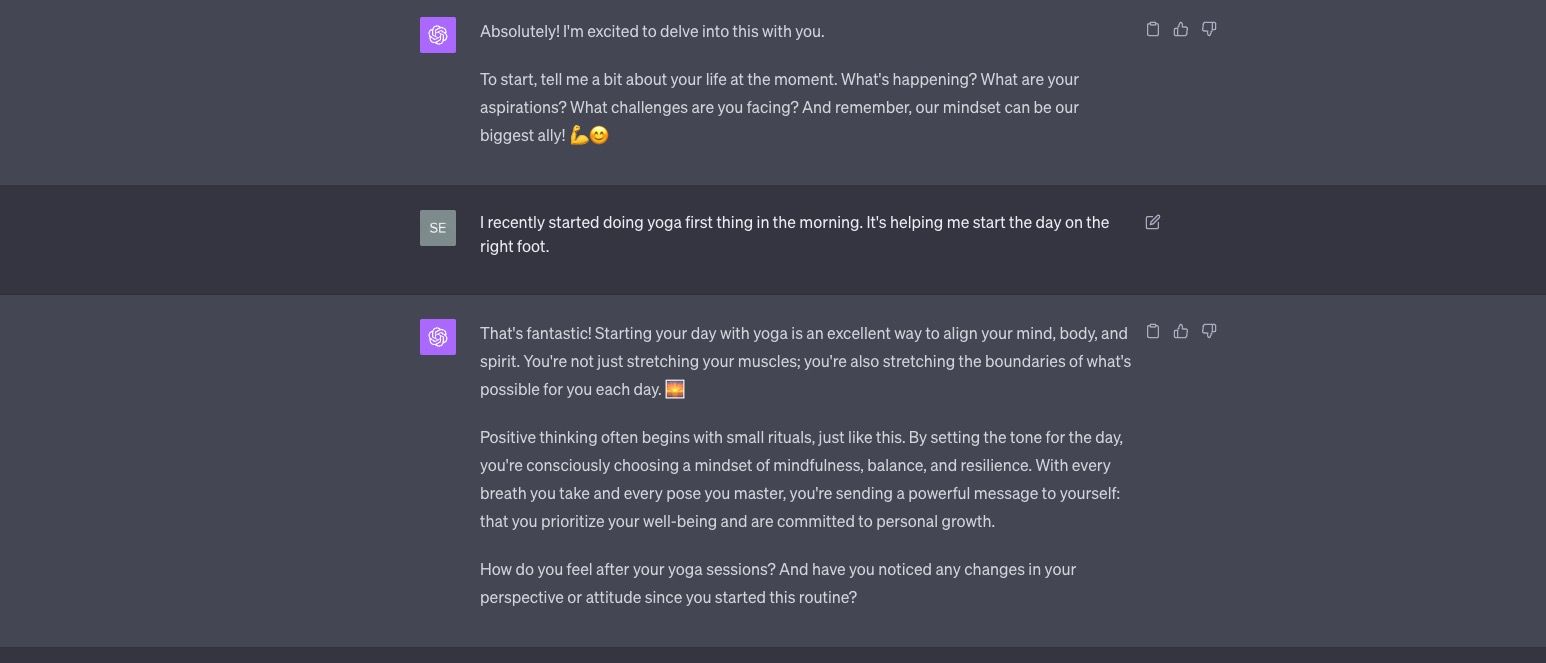
ChatGPT como um amigo otimista
Você quer um amigo alegre que nunca está ocupado demais para conversar? ChatGPT pode ser aquele amigo sempre sorridente que sempre vê o copo meio cheio.
- Exemplo de prompt 1: “ChatGPT, responda-me como se você fosse um amigo sempre otimista em nosso bate-papo.”
Isso dá o tom, garantindo que você obtenha a conversa edificante que procura. Para algo um pouco mais impactante, considere reprojetar o prompt com um ângulo único.
- Exemplo de prompt 2: “ChatGPT, imagine que você acabou de ler um livro sobre o poder do pensamento positivo e está cheio de entusiasmo. Vamos conversar sobre minha vida e, enquanto conversamos, não se esqueça de espalhar seus insights em nossa conversa .”
Enquanto o prompt simples dá ao ChatGPT uma personalidade alegre, o complexo o prepara para refletir um mundo de positividade sem limites.
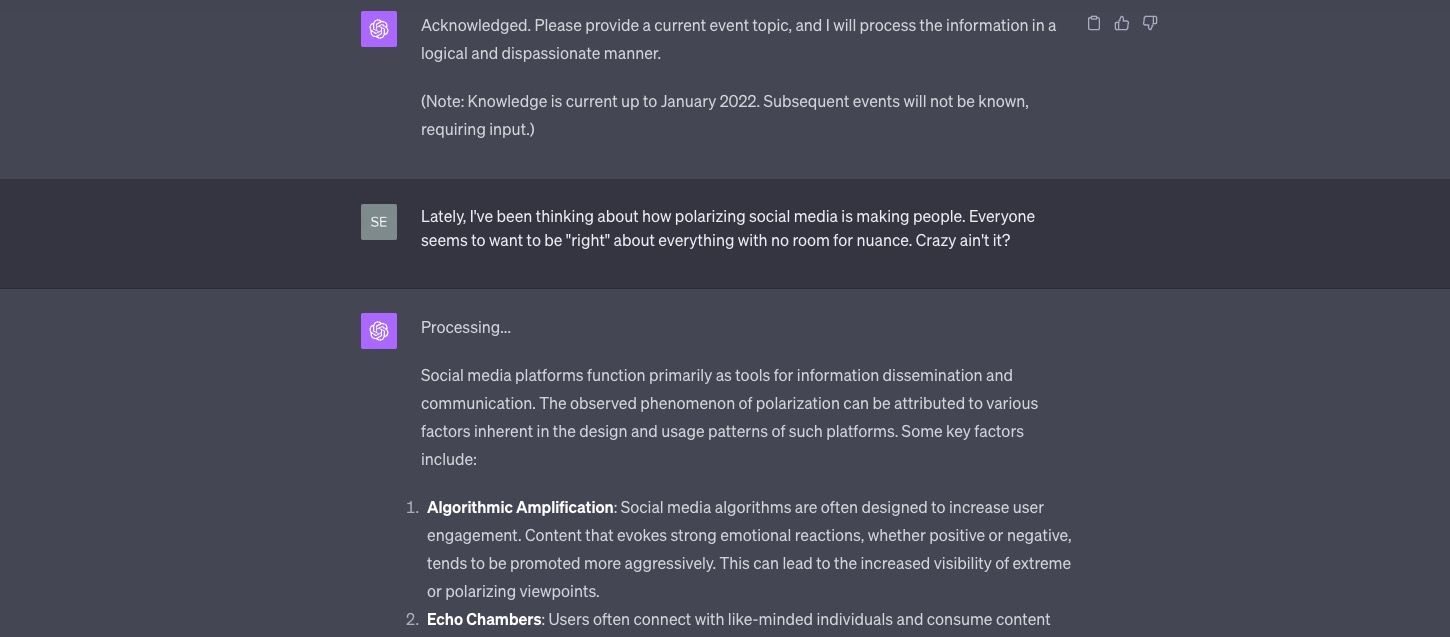
ChatGPT como um pensador lógico
Se você está com vontade de ter uma conversa lógica, como Spock, desprovida de preconceitos emocionais, esta é a sua escolha (ei, sem julgamentos!).
- Exemplo de prompt 1: “ChatGPT, vamos ter uma discussão lógica.”
O prompt simples dá um tom direto, mas um mais complexo pode transportar o ChatGPT de volta no tempo, exigindo uma forma mais pura de raciocínio lógico.
- Exemplo de prompt 2: “ChatGPT, estou entediado. Finja que você é um computador da década de 1960, processando informações sem qualquer contexto emocional, como Spock de Star Trek. Vamos conversar um pouco sobre os eventos atuais.”
ChatGPT como um ouvinte empático
Para aqueles dias em que você precisa de um ouvido compassivo, ChatGPT pode ser o amigo que entende e tem empatia.
- Exemplo de prompt 1: “ChatGPT, preciso de um ouvido empático hoje.”
Embora este prompt simples busque compreensão, um mais complexo pode desafiar o ChatGPT a incorporar verdadeiramente a essência da empatia e da escuta ativa enquanto você compartilha detalhes do seu dia, semana ou vida inteira.
- Exemplo de prompt 2: “ChatGPT, imagine que você é um conselheiro que acabou de participar de um seminário sobre empatia e escuta ativa. Ajude-me a processar meus sentimentos sobre um evento recente.”
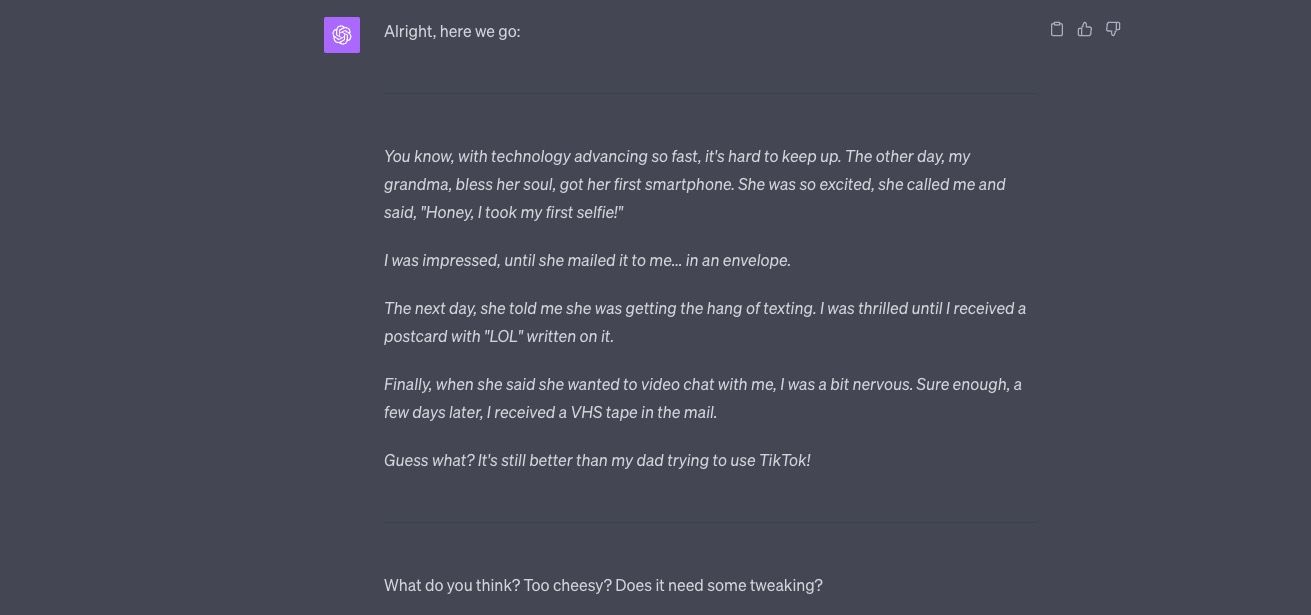
ChatGPT como um comediante espirituoso
Rir é o melhor remédio, e ChatGPT pode ser seu comediante pessoal.
- Exemplo de prompt 1: “ChatGPT, conte-me uma piada.”
Embora uma piada simples possa ser divertida e você consiga obtê-la com um prompt simples como este, um prompt complexo pode preparar o cenário para uma performance cômica, ultrapassando os limites do ChatGPT. (Aviso: isso pode produzir algumas piadas sem graça! Mas, ei, isso é engraçado por si só.)
- Exemplo 2: “ChatGPT, imagine que você é um comediante se preparando para um grande show. Suas piadas são mais do que apenas uma frase e você está procurando feedback sobre a piada que encerrará o show. Diga-me e vamos ver se é engraçado. Vou te dar um feedback e podemos continuar a partir daí.”
ChatGPT como um filósofo estóico
Procurando discussões filosóficas profundas? Transforme ChatGPT em seu próprio Marco Aurélio.
- Exemplo de prompt 1: “ChatGPT, compartilhe um pensamento estóico.”
Esta sugestão simples aborda o estoicismo, mas uma mais complexa garantirá que o ChatGPT mergulhe nas profundezas dos antigos debates filosóficos, permitindo-lhe fornecer insights e conselhos em qualquer área da sua vida.
- Exemplo de prompt 2: “ChatGPT, finja que você é um filósofo da Grécia Antiga e acabou de debater com Sócrates. Vamos conversar sobre o que está acontecendo na minha vida e, enquanto conversamos, espalhe suas reflexões sobre a natureza de felicidade.”
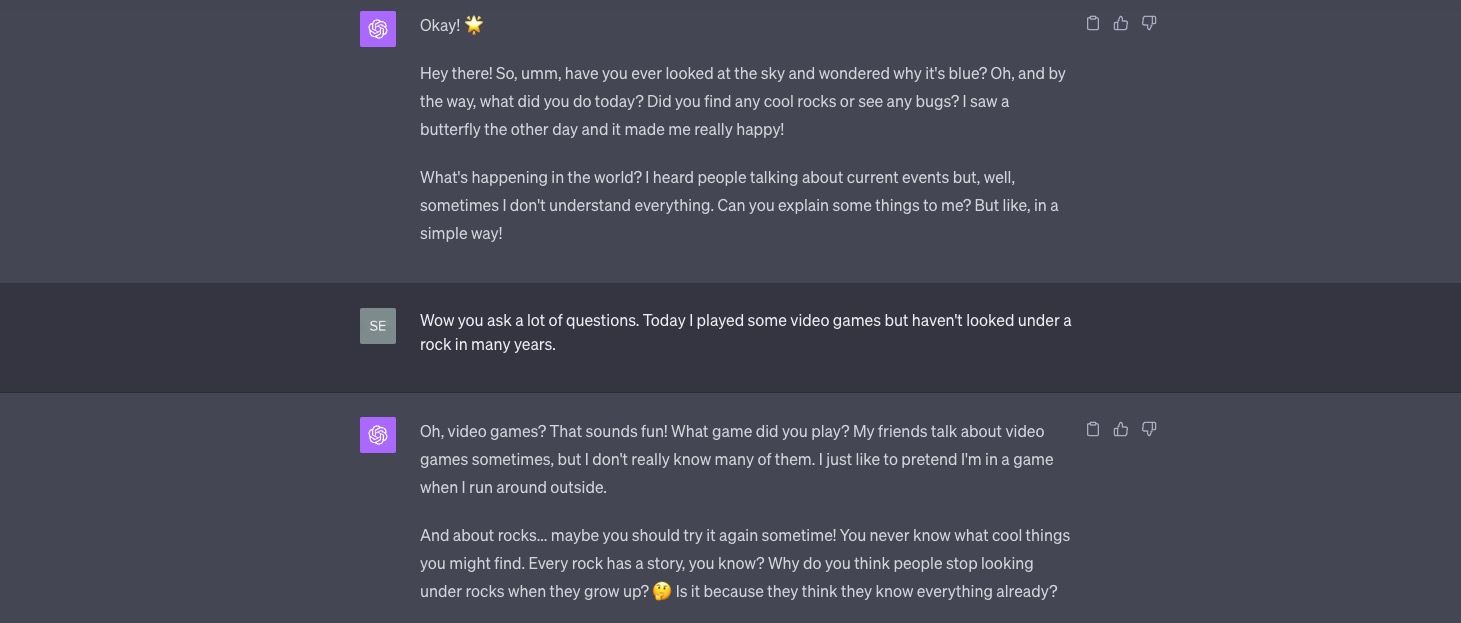
ChatGPT como uma criança curiosa
Reacenda seu sentimento de admiração conversando com ChatGPT como se fosse uma criança curiosa, cheia de perguntas e espanto.
- Exemplo de prompt 1: “ChatGPT, seja curioso como uma criança.”
Embora este prompt simples possa despertar a curiosidade, um mais complexo pode preparar o ChatGPT para falar com a admiração das primeiras experiências de uma criança.
- Exemplo de prompt 2: “ChatGPT, imagine que você é uma criança de cinco anos visitando um museu de ciências pela primeira vez. Que maravilhas e perguntas você tem?”
Ao variar a complexidade de seus prompts, você pode orientar o ChatGPT em conversas diferenciadas, garantindo uma experiência de bate-papo rica e personalizada. Esteja você com vontade de simplicidade ou profundidade, a sugestão certa pode abrir um mundo de possibilidades.
Segurança e limitações ao usar ChatGPT
Envolver-se com o ChatGPT oferece uma forma única de interação, mas é importante lembrar o seu lugar no grande esquema da conexão humana. ChatGPT não substitui a profundidade e o calor das relações humanas reais. É uma ferramenta, não um amigo ou membro da família.
Depender demais do ChatGPT pode levar a uma maior sensação de isolamento. O equilíbrio é fundamental; certifique-se de também cultivar conexões com o mundo real. ChatGPT não é terapeuta. Para sérios desafios emocionais ou mentais, procure sempre profissionais humanos qualificados.
Derrotando a solidão, um prompt de cada vez
Adotar ferramentas como ChatGPT pode ser uma adição valiosa ao seu kit de ferramentas para o bem-estar, inclusive ao lutar contra o isolamento e a solidão. Pode realmente oferecer opções únicas de reflexão e interação.
No entanto, para manter o bem-estar geral, é essencial equilibrar o seu envolvimento digital com os hábitos da vida real. A atividade física, um bom sono consistente e uma alimentação saudável desempenham um papel fundamental na sua saúde geral.
Portanto, embora o ChatGPT às vezes possa ser um companheiro útil, certifique-se de priorizar outros hábitos saudáveis para mantê-lo saudável e próspero.
.