.
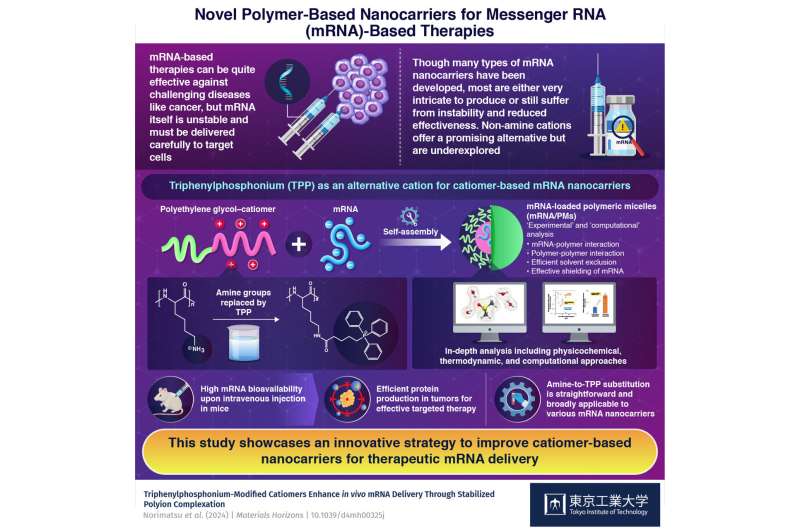
Este estudo mostra uma estratégia inovadora para melhorar nanocarreadores baseados em catiômeros para entrega terapêutica de mRNA. Crédito: Tokyo Tech
Entre as maneiras vastamente diferentes de lidar com uma doença, controlar a expressão genética das células é, sem dúvida, uma das mais poderosas. Nas últimas décadas, os cientistas criaram dezenas de estratégias inovadoras que envolvem o uso de RNA mensageiro (mRNA) para “forçar” as células a construir proteínas específicas. Essas terapias baseadas em mRNA ganharam destaque recentemente como vacinas contra doenças infecciosas como a COVID-19. Além disso, elas têm potencial significativo para tratar câncer e distúrbios genéticos.
Como o mRNA em si é bastante instável e facilmente destruído por enzimas no corpo, as terapias baseadas em mRNA dependem de técnicas de administração de medicamentos; a ideia central é encapsular e proteger moléculas de mRNA dentro de nanoestruturas que podem colocá-las com segurança dentro das células-alvo. Hoje, os nanocarreadores de mRNA mais explorados são feitos de lipídios catiônicos ou polímeros contendo amina, que formam pequenas esferas protetoras que podem se difundir nas células para liberar sua carga. No entanto, os designs existentes ainda enfrentam problemas de estabilidade, o que aumenta os custos e leva a doses mais altas para obter o efeito desejado.
Neste contexto, uma equipe de pesquisa do Japão explorou uma alternativa aos materiais baseados em amina como nanocarreadores de mRNA. Em seu último estudo, publicado em Horizontes de materiaisos pesquisadores investigaram o potencial do trifenil fosfônio (TPP) como um substituto para os grupos amina usados como cátions para formar micelas carregadas de mRNA.
“Cátions baseados em fosfônio fornecem propriedades iônicas únicas que favorecem interações com ânions como mRNA, como sua distribuição de carga e força de ligação aos ânions, que derivam de diferenças na eletronegatividade entre fósforo e nitrogênio”, explica o professor associado Yasutaka Anraku do Instituto de Tecnologia de Tóquio, que liderou o estudo. “Além disso, suas três frações fenil facilitam interações hidrofóbicas, levando à complexação estável de mRNA. Assim, substituir aminas por TPP pode aumentar a eficiência de entrega de mRNA”, ele acrescenta.
Para testar sua hipótese, os pesquisadores projetaram micelas poliméricas usando polietilenoglicol (PEG), TPP e mRNA. Primeiro, eles desenvolveram uma estratégia altamente eficiente para substituir os grupos amina em copolímeros de PEG-poli(L-lisina) por TPP. Os polímeros resultantes naturalmente se automontam em uma estrutura núcleo-casca em condições enriquecidas com ânions devido à sua hidrofobicidade e distribuição de carga. Além disso, dado que o mRNA contém muitos fosfatos carregados negativamente, os grupos TPP positivos os atraem para se automontarem, garantindo uma carga de mRNA alta e estável nas micelas.
A estratégia deles foi cuidadosamente avaliada e verificada por meio de uma análise abrangente, incluindo abordagens termodinâmicas, físico-químicas e computacionais. Além disso, eles também testaram as capacidades do sistema proposto para entregar mRNA a células tumorais in vivo usando um modelo de camundongo.
“Após injeção intravenosa, micelas portadoras de TPP resultaram em um aumento notável na biodisponibilidade do mRNA, facilitando a produção eficiente de proteína em tumores sólidos”, destaca Anraku. Notavelmente, os experimentos revelaram que os níveis de mRNA intactos restantes no sangue após 30 minutos foram ordens de magnitude maiores ao usar as micelas baseadas em TPP propostas em vez das baseadas em amina. Da mesma forma, a expressão de proteína em tecidos tumorais foi mais de 10 vezes maior ao usar micelas baseadas em TPP.
No geral, parece que essa estratégia inovadora tem muito potencial no campo da terapêutica de mRNA, que inclui a administração direcionada de medicamentos.
“Dado que micelas poliméricas podem ser direcionadas a tecidos específicos anexando ligantes, micelas poliméricas portadoras de TPP podem servir como uma plataforma robusta para entrega de mRNA em vários tecidos”, diz Anraku. Com alguma sorte, essa tecnologia abrirá caminho para o tratamento eficaz das doenças mais desafiadoras da humanidade.
Mais Informações:
Jumpei Norimatsu et al, catiômeros modificados com trifenilfosfônio melhoram a administração de mRNA in vivo por meio da complexação de poliíons estabilizados, Horizontes de materiais (2024). DOI: 10.1039/D4MH00325J
Fornecido pelo Instituto de Tecnologia de Tóquio
Citação: Melhorando o design de nanocarreadores carregados com mRNA para terapias direcionadas (2024, 22 de julho) recuperado em 22 de julho de 2024 de https://phys.org/news/2024-07-mrna-nanocarriers-therapies.html
Este documento está sujeito a direitos autorais. Além de qualquer uso justo para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins informativos.
.