.

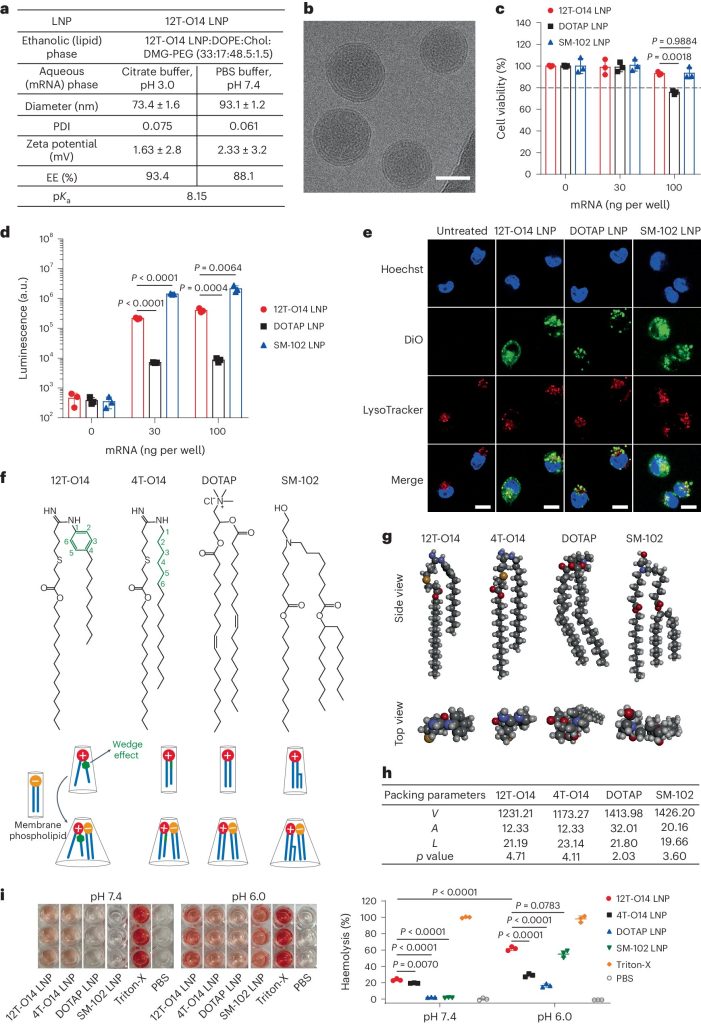
Caracterização e avaliação in vitro de 12T-O14 LNP. Crédito: Química da Natureza (2024). DOI: 10.1038/s41557-024-01557-2
Imagine um cenário em que um hacker habilidoso precisa carregar um software crítico para atualizar um servidor central e impedir que um vírus potencialmente letal cause estragos em uma vasta rede de computadores. O programador, armado com o código que salva vidas, precisa navegar por um território traiçoeiro repleto de adversários, e o sucesso depende de obter prontamente um veículo de entrega seguro e furtivo que possa colocar o hacker exatamente onde ele precisa estar.
No contexto da medicina moderna, o RNA mensageiro (mRNA) serve como hacker, carregando instruções genéticas para produzir proteínas específicas dentro das células que podem induzir respostas imunes desejadas ou sequestrar elementos celulares mal-adaptativos. As nanopartículas lipídicas (LNPs) são os veículos de entrega furtivos que transportam essas moléculas frágeis de mRNA pela corrente sanguínea até suas células-alvo, superando as defesas do corpo para entregar sua carga útil com segurança e eficiência.
No entanto, assim como a construção de um veículo furtivo avançado, a síntese de lipídios catiônicos — um tipo de molécula lipídica com carga positiva e um componente essencial dos LNPs — costuma ser um processo demorado, envolvendo várias etapas de síntese química e purificação.
Agora, Michael Mitchell e uma equipe da Universidade da Pensilvânia abordaram esse desafio com uma nova abordagem que alavanca uma técnica de fabricação de biblioteca composta conhecida como “química do tipo clique” para criar LNPs em uma única e simples etapa. Suas descobertas, publicadas no periódico Química da Naturezamostram que esse método não apenas acelera o processo de síntese, mas também apresenta uma maneira de equipar esses veículos de entrega com um “GPS” para atingir melhor órgãos específicos, como fígado, pulmões e baço, potencialmente abrindo novos caminhos para o tratamento de uma série de doenças que surgem nesses órgãos.
“Desenvolvemos o que chamamos de lipídio degradável incorporado com amidina (AID), uma molécula biodegradável de estrutura única”, diz Mitchell. “Pense nisso como um veículo de mRNA personalizado e fácil de construir com um kit corporal que informa seu sistema de navegação. Ao ajustar sua forma e degradabilidade, podemos melhorar a entrega de mRNA nas células de forma segura. Ao ajustar a quantidade de lipídio AID que incorporamos ao LNP, também podemos guiá-lo para diferentes órgãos do corpo, muito parecido com programar diferentes destinos em um GPS.”
O primeiro autor, Xuexiang Han, ex-pesquisador de pós-doutorado no Laboratório Mitchell, explica que sua nova abordagem permite a criação rápida de diversas estruturas lipídicas em apenas uma hora, em comparação com o processo de semanas tradicionalmente necessário.
“O resultado é uma aceleração significativa no desenvolvimento e teste de AID-lipídios”, ele diz. “Isso nos permitirá explorar uma gama mais ampla de composições de lipídios e seus efeitos na entrega de mRNA.”
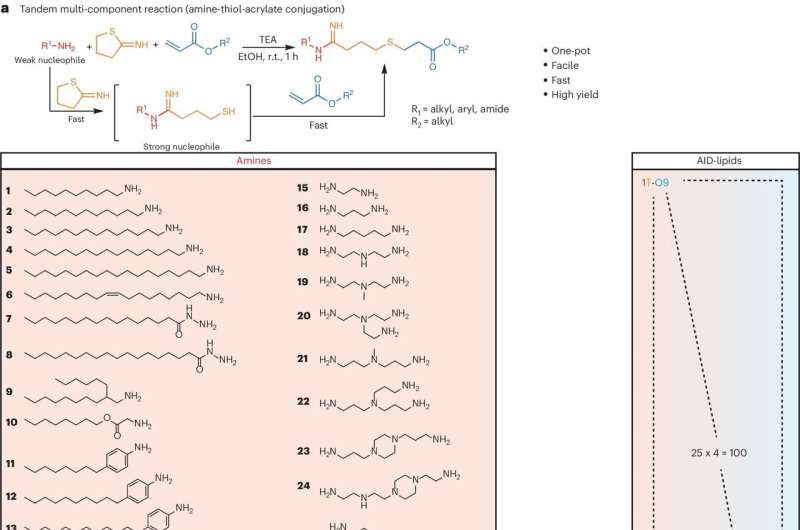
Síntese rápida e fácil de AID-lipídios via T-MCR para entrega de mRNA. a, T-MCR baseado na conjugação amina–tiol–acrilato entre aminas, reagente de Traut e alquil acrilatos. O esquema de reação e mecanismo de T-MCR, bem como as estruturas químicas de aminas 1–25 e alquil acrilatos O9–O16 são mostrados. b, Esquema da formulação e aplicação de LNPs carregados com mRNA. LNPs formulados com AID-lipídios mediam a entrega de vacinas baseadas em mRNA, bem como a substituição de proteínas e terapêuticas de edição genética para tecidos-alvo. O esquema em b foi criado com BioRender.com. Crédito: Química da Natureza (2024). DOI: 10.1038/s41557-024-01557-2
Para atingir essas construções aceleradas de lipídios AID, os pesquisadores fizeram uso de uma reação multicomponente em tandem (T-MCR) para sintetizar os lipídios AID, um processo que envolve a combinação de compostos químicos – uma amina, tiol e acrilato – em uma única etapa para produzir diversas estruturas lipídicas rapidamente. A abordagem de síntese one-pot reduz significativamente o tempo necessário para produzir lipídios catiônicos, tornando-a uma solução mais eficiente e escalável para entrega de mRNA-LNP.
A equipe de Mitchell sintetizou 100 AID-lipídios diferentes, que foram então formulados em LNPs. Os LNPs resultantes foram testados quanto à sua capacidade de entregar mRNA a vários órgãos em modelos animais, o que mostrou à equipe que eles poderiam atingir órgãos específicos com alta precisão.
Uma característica fundamental desses AID-lipídios é sua capacidade de incorporar componentes degradáveis, garantindo que os LNPs se quebrem com segurança dentro do corpo após entregar sua carga útil de mRNA. Essa biodegradabilidade é essencial para minimizar potenciais efeitos colaterais e garantir que os agentes terapêuticos não se acumulem no corpo ao longo do tempo. Os pesquisadores demonstraram que os AID-lipídios LNPs poderiam efetivamente entregar mRNA codificando proteínas funcionais, destacando seu potencial para uso em uma ampla gama de aplicações terapêuticas.
Outra descoberta significativa foi a identificação de uma estrutura distinta de anel de cabeça (ou cauda)-alquil anilina que se mostrou particularmente eficaz em melhorar a entrega de mRNA. Essa estrutura, que a equipe apelidou de “efeito cunha”, permite que os LNPs penetrem nas membranas celulares de forma mais eficiente, facilitando a liberação de mRNA nas células-alvo. O estudo mostrou que os LNPs com essa estrutura alcançaram maiores eficiências de transfecção e maiores níveis de expressão de proteína em comparação aos LNPs sem essa estrutura.
Os pesquisadores também exploraram o potencial dos LNPs AID-lipídicos para administrar vacinas de mRNA visando células imunes específicas e demonstraram que esses LNPs poderiam transfectar seletivamente células apresentadoras de antígenos no baço, uma etapa crítica para induzir respostas imunes robustas.
“Essa descoberta abre novas possibilidades para o desenvolvimento de vacinas baseadas em mRNA que podem atingir e ativar precisamente o sistema imunológico, potencialmente levando a uma imunidade mais eficaz e duradoura contra várias doenças”, diz Han.
À medida que Mitchell e a equipe continuam a refinar sua plataforma, eles estão se concentrando em uma segmentação ainda mais precisa, especialmente nos pulmões.
“Estamos agora trabalhando para guiar nossos veículos além da barreira inicial de vasos sanguíneos para alcançar mais profundamente o tecido pulmonar”, diz Mitchell. “É um pouco como programar nosso sistema de entrega para navegar por camadas de segurança cada vez mais complexas.”
Mais Informações:
Xuexiang Han et al, Síntese rápida e fácil de lipídios degradáveis incorporados com amidina para administração versátil de mRNA in vivo, Química da Natureza (2024). DOI: 10.1038/s41557-024-01557-2
Fornecido pela Universidade da Pensilvânia
Citação: Equipe é pioneira em uma ‘plataforma única’ para produzir prontamente partículas de entrega de mRNA (2024, 9 de julho) recuperado em 9 de julho de 2024 de https://phys.org/news/2024-07-team-pot-platform-promptly-mrna.html
Este documento está sujeito a direitos autorais. Além de qualquer uso justo para fins de estudo ou pesquisa privada, nenhuma parte pode ser reproduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins informativos.
.